
コンテンツ
序論:脳卒中後筋力低下の多因子性と臨床的課題
脳卒中リハビリテーションの臨床現場において、我々が対峙する筋力低下は、単一の要因では説明できない複雑な病態を呈します。この筋機能不全は、一次的には上位運動ニューロンの損傷に起因する中枢神経系の機能障害として理解されますが、その機能的帰結は運動単位の動員不全や発火頻度の低下といった中枢性の要因のみに帰結するものではありません。
近年の研究は、中枢神経系の損傷に加え、麻痺した筋組織そのものに生じる二次的な筋固有特性の変化が、筋力低下の重要な決定因子であることを示唆しています。これらの変化には、①筋萎縮や線維長の短縮といった構造的適応と、②筋活動レベルに応じて力発揮の最適長が変化する動的特性の両側面が含まれます。
本稿では、この多因子的な病態生理を統合的に理解するために、まず正常な筋における力発揮の基本原則、特に最大下収縮時における動的な長さ-張力関係を解説します。次に、動物実験モデルから明らかになった、慢性的な長さ変化に対する筋の構造的可塑性、すなわちサルコメアの適応的変化を詳述します。続いて、これらの基礎的知見が、脳卒中患者において特有の機能障害として、いかに臨床的に実証されているかを示してきます。
この一連の科学的知見を統合することで、筋の構造的・動的特性と中枢神経系の両者に働きかけるハンドリングが、なぜ論理的かつ不可欠な治療戦略となりうるのか、その科学的根拠を構築していきます。
筋張力発生の基本原則とその動的性質
脳卒中後の筋機能不全を理解するためには、まず正常な筋がどのように力を生み出し、制御しているのか、その基本的な原則を把握する必要があります。筋が発揮する力は、単純なオン・オフのスイッチではなく、筋の長さや活動レベルといった複数の要因によって精密に調整されています。この章では、その静的および動的な基本原則を解説します。
静的モデル:古典的「長さ-張力関係」の理論
筋が発揮できる力は、その収縮を開始する時の筋の長さに大きく依存します。この普遍的な原則は「長さ-張力関係」として知られています。
この関係の鍵を握るのは、筋線維の最小単位である「サルコメア」です。サルコメア内部では、アクチンとミオシンという2種類のフィラメントが重なり合っており、ミオシンがアクチンに結合(クロスブリッジを形成)することで張力が発生します。したがって、筋が発揮できる能動的な張力は、形成可能なクロスブリッジの数に比例します。
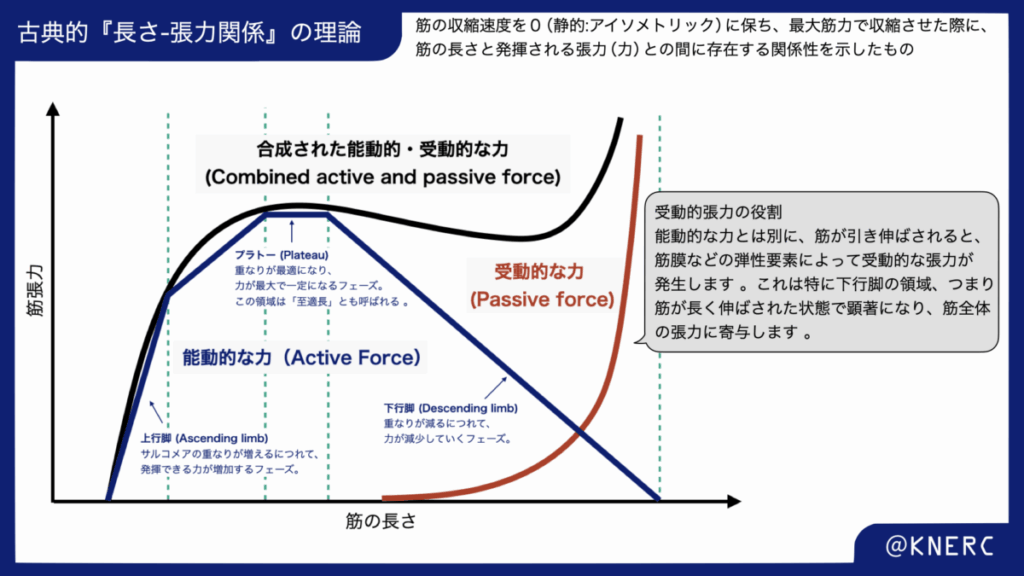
この古典的モデルは、最大努力で筋が収縮する際の、いわば「静的な設計図」を示しています。
動的モデル:活動レベル依存的な最適筋長のシフト
しかし、私たちの日常動作の多くは、最大努力ではない最大下収縮で行われます。Zimmermannらが発表したレビュー論文では、この最大下収縮の際に古典的な「長さ-張力関係」が動的に変化する「長さ依存性の活性化」という現象が詳述されています。
これは、筋への神経刺激が弱い(=活性化レベルが低い)ほど、最大の力を発揮できる至適筋線維長が、より伸張された側(長い筋長)にシフトする現象です。Bohmらの研究では、ヒトのヒラメ筋において、最大筋電活動(100% EMGmax)時と比較して、30%の活動レベルでは至適長が平均で約9%長くなることが実験的に示されました。
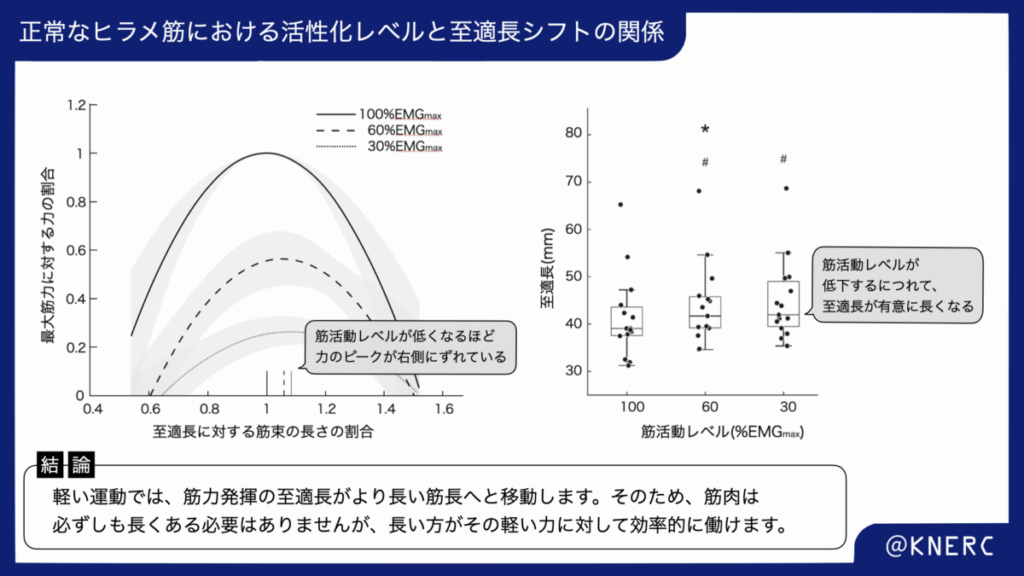
このシフトが生じる主なメカニズムは、筋線維が伸張されることに伴うカルシウム感受性の増大にあると考えられています。筋線維が長くなると、アクチンとミオシン間の物理的な距離(ミオフィラメント格子間隔)が縮小します。この距離が縮まることで、筋収縮の引き金となるカルシウムイオン(Ca²⁺)が効率よく作用し、結果として弱い神経刺激でも比較的大きな張力を発生させることが可能になります。
この「長さ依存性の活性化」は、正常な筋が多様な状況下で効率的に力を制御するための、洗練された動的な生理学的メカニ-ズムです。この動的な力発揮特性の理解は、脳卒中後の筋機能変化を考察する上で不可欠な基準となります。
筋の構造的可塑性:慢性的な長さ変化への適応と不適応
正常な筋が持つ動的な力発揮特性に対し、脳卒中後の麻痺した筋では、二次的に物理的な構造変化が生じることが報告されています。筋肉は、単に与えられた長さに受動的に存在するのではなく、慢性的に置かれた環境に応じて自らの構造を積極的に変化させる高い可塑性を持っています。この章では、その適応と不適応のメカニズムを、基礎的な動物実験と、それが脳卒中後の筋にどう現れるかという臨床的知見から解説します。
基礎的証拠:不動に対するサルコメア数の適応的変化
筋肉が慢性的な長さの変化にどのように適応するのか、その根底にあるメカニズムは、Williams & Goldspinkらが行った動物実験モデルによって明らかにされました。彼らの研究では、関節をギプスで固定し、筋を特定の長さに保持すると、筋線維を構成するサルコメアの数が変化することが示されました。
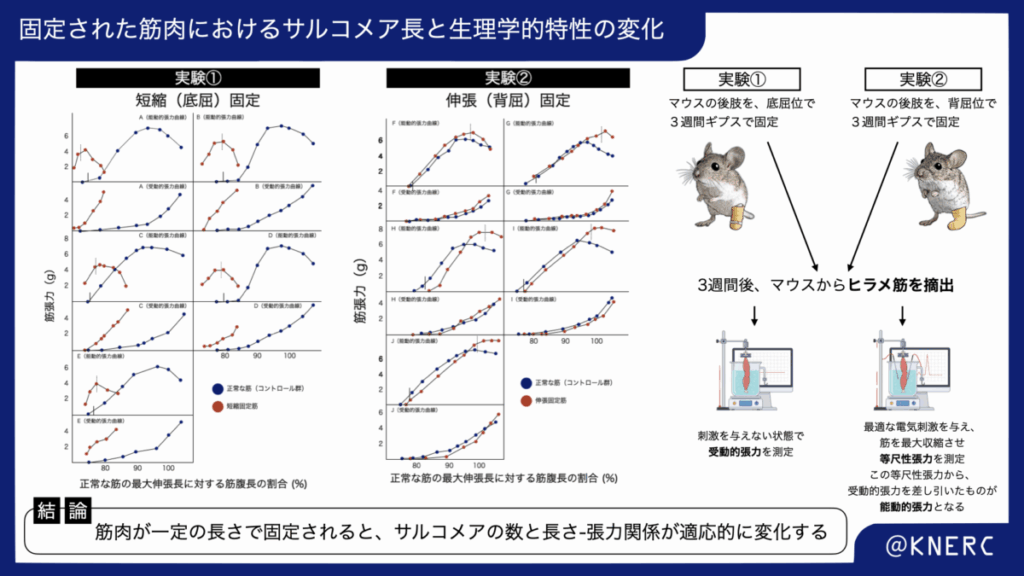
脳卒中後に生じる筋組織の構造的変化
動物実験で示されたサルコメアレベルでの適応は、脳卒中後に生じる痙縮や不動によって、麻痺した筋における二次的な構造変化として現れます。Grayらの包括的なレビューは、これらの変化が筋力低下の直接的な原因となりうることを示しており、主に以下の4点に集約されます。
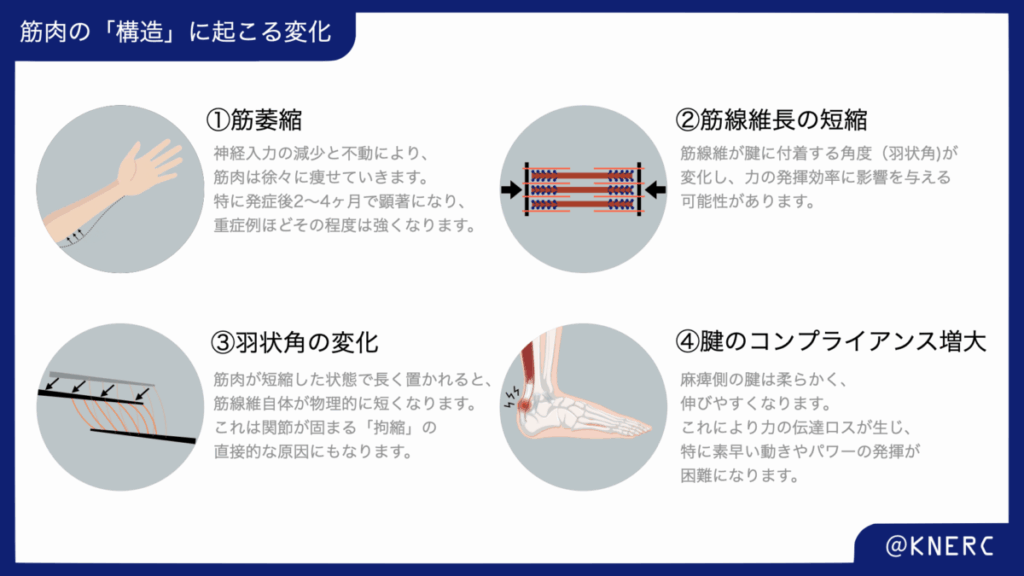
これらの構造的変化は、それぞれが独立して、また相互作用しながら、麻痺した筋肉の力発揮能力を低下させます。
次の章では、これらの変化が総合的にどのような機能的帰結をもたらすのかを詳述します。
脳卒中後片麻痺患者における機能的帰結
第2部で詳述した筋組織の構造的適応は、単なる組織学的変化に留まらず、麻痺した筋の力発揮特性を根本的に変容させます。この章では、これらの構造変化が臨床的にどのような機能的帰結をもたらすのか、ヒトの研究データに基づいて多角的に実証します。
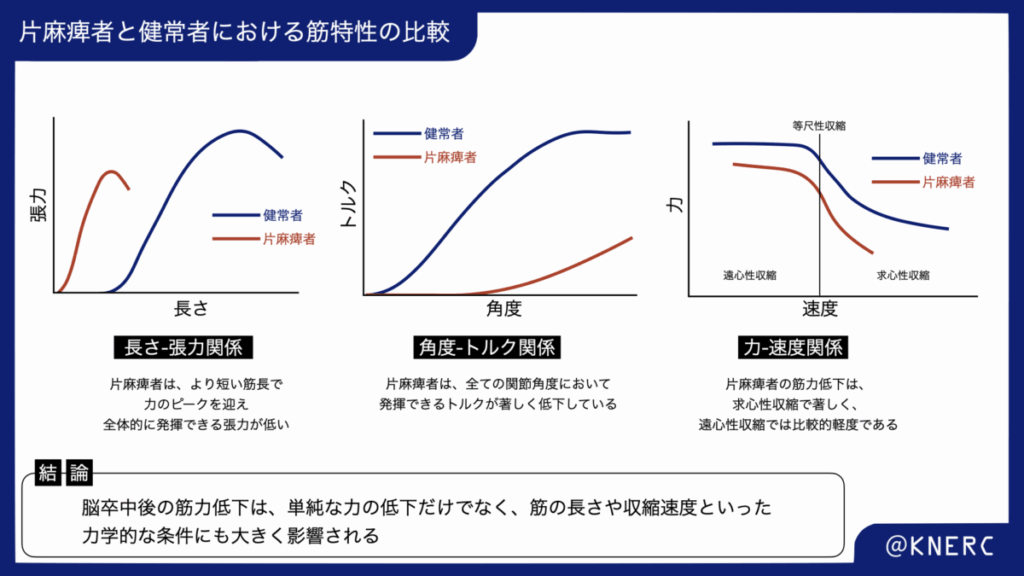
長さ-張力関係の変化:短縮域での選択的筋力低下
動物実験で示されたサルコメア数の適応は、長さ-張力曲線のシフトとして現れます。Grayらのレビュー論文では、特に短縮適応した筋において、この機能的帰結が「長さ-張力曲線の左方移動」として最も明確に表現されています。これは、麻痺した筋肉が正常な筋肉と比較して、より短い筋線維長で張力のピークを迎えるようになったことを意味します。このシフトの結果、特に筋が最も短くなる肢位(短縮域)において、著しいトルク産生能力の低下が生じます。
この「短縮域での選択的筋力低下」という仮説は、AdaらやKooらによる研究によって実験的に証明されています。彼らの研究は、脳卒中患者のトルク-角度曲線の「形状」そのものが健常対照群と異なっていることを明らかにし、この機能障害が一次的な筋力産生機構そのものの変容に起因することを示唆しています。
力-速度関係の変化と収縮様式による違い
筋機能の低下は、筋の長さに加えて「収縮速度」の次元でも理解する必要があります。
筋力低下の複合的要因の考察
したがって、脳卒中後の筋力低下は単一の要因では説明できず、複合的な病態生理として理解する必要があります。Grayらのレビューで示されているように、この機能障害は以下の要因が相互作用した結果と考えられます。
これら二つの要因は、互いに影響を及ぼし合う悪循環を形成する可能性があります。例えば、中枢性の問題で筋を十分に動かせないことが二次的な構造変化を招き、その構造変化がさらに効率的な力発揮を困難にし、さらなる不使用を助長するといった具合です。この複合的な視点が、効果的なリハビリテーション戦略を立案する上で不可欠となります。
科学的根拠に基づく臨床推論と実践
これまでに概説した筋の動的・構造的変化は、臨床における評価や治療介入に対して重要な示唆を与えます。第1部から第3部で構築した科学的根拠は、我々が日常的に行っている介入、特に徒手的なアプローチの理論的背景を強固にするものです。この章では、これらの知見を統合し、具体的な臨床推論と実践に繋げます。
評価と運動選択における示唆
KooらやAdaらの研究で示されたように、脳卒中後の筋肉は短縮域で選択的な筋力低下を呈し、トルク-角度曲線の「形状」そのものが健常対照群とは異なっています。これらの知見は、単一の肢位での筋力評価の限界を示唆しており、この長さ-張力関係の変化が筋力低下の重要な要因であると結論付けられています。患者の機能的な困難さ(例:立脚初期の膝折れ、リーチ動作での最終伸展困難)を真に理解するためには、可動域全体にわたる筋の反応や張力の変化を評価することが不可欠です。
この「関節角度依存性の筋力低下」という特性は、リハビリテーションにおける運動療法の選択にも直結します。Pedrosaらが示すように、筋長と可動域の相互作用を考慮した運動選択は、効果的な介入の鍵となります。例えば、短縮域で筋力低下を呈する筋に対しては、その特定の運動範囲をターゲットとした筋力増強運動が論理的な帰結となります。単に「筋力を強化する」のではなく、「どの範囲の筋力を強化する必要があるのか」を明確にすることが、より的確で包括的なリハビリテーション戦略の立案に不可欠です。
ハンドリングの理論的根拠と実践
麻痺筋が呈する多因子的な病態に対し、セラピストによるハンドリングは、筋の構造的・生理学的特性と中枢神経系の両者に働きかける、極めて合理的なアプローチとして位置づけられます。本稿で解説してきた複数の科学的知見によって支持されるその臨床指針は、以下の3つの側面に集約されます。
①構造的適応への介入:筋線維長の再構築
脳卒中後の筋の短縮は、サルコメア数の減少という物理的な構造変化に起因します。これに対しハンドリングは、持続的な伸張や適切な肢位での運動誘導を通じて、構造的問題である筋線維長を確保することを目的とします。この徒手的な介入は、短縮した筋にサルコメア数の増加を促すための直接的な機械的刺激となり、筋の柔軟性と長さを回復させ、変容した長さ-張力曲線を正常な状態に近づけるための根本的なアプローチです。
②動的特性への介入:短縮域での力発揮の再学習
麻痺筋では「長さ-張力関係」という動的な力発揮特性そのものが変容しているため、患者が自力では十分な筋活動を生成できない機能的短縮域において、弱点である短縮位での力発揮を促すようにハンドリングする。具体的には、目的とする関節運動の安定性を確保し、適切な触覚的・固有受容感覚的手がかりを与えることで、その運動範囲における運動単位の動員を最大化する。中間域から最終域への段階的な収縮誘導や、最終域での等尺性収縮課題は、成功体験を重ねる上で有効である。これにより、変化してしまった筋の動的特性に応じた、効率的な力発揮パターンを再学習させる。
麻痺筋では、「長さ-張力関係」という動的な力発揮特性そのものが変容しています。ハンドリングは、患者が自力では十分な筋活動を生成できない機能的短縮域において、弱点である短縮位での力発揮を促すことを目指します。徒手的な促通によって、その長さで適切な活動レベルでの収縮を経験させることは、変化してしまった筋の動的特性を再学習させる機会を提供します。
③中枢神経系への介入
脳卒中後の筋力低下は中枢神経系の要因と筋固有特性の変化が複合した結果であり、ハンドリングは運動に伴う質の高い感覚入力を提供し、神経系の再学習を促します。特に、比較的保たれた遠心性収縮能を活用し、神経系の運動学習を促すようにハンドリングすることは有効な戦略です。相対的に保たれやすい遠心性収縮を丁寧に誘導することは、運動のコントロールを学習させると同時に、運動に伴う固有受容感覚入力を増強・最適化する。この質の高い感覚フィードバックが、運動制御に関わる中枢神経系の可塑性を促し、運動の内部モデルを修正する上で重要な役割を果たします。
したがって、ハンドリングは予め定められた手順の適用ではありません。それは、筋の構造的可塑性、動的特性、そして神経制御に関する科学的根拠を臨床推論の基盤とし、患者個々の病態に応じて最適化される、論理的な治療戦略なのです。
結論
本稿では、脳卒中後の筋力低下が、単に中枢神経系の損傷に起因する問題だけでなく、麻痺した筋組織そのものに生じる動的・構造的な適応(不適応)が深く関与する、多因子的な病態であることを詳述しました。
正常な筋が持つ「長さ依存性の活性化」という動的な力発揮特性を基盤とし、慢性的な長さ変化に対する「サルコメア数の適応」という構造的可塑性を経て、最終的に長さ-張力曲線が左方へ移動します。これにより、特に筋肉が短縮された肢位で選択的な筋力低下を呈するという、特有の機能障害が引き起こされることが、実験的にも証明されています。
この一連の科学的根拠は、単一の肢位での筋力評価や、画一的な運動療法の限界を示唆するものです。したがって、徒手的介入(ハンドリング)とは、本稿で提示した科学的根拠を臨床推論の基盤とし、患者個々の病態に応じて最適化される、論理的な治療戦略そのものであると言えます。それは、筋の構造、動的特性、そして神経制御の各要素を再統合し、患者の機能的な運動能力を再構築するための、科学的根拠に基づいた治療体系です。
Q&A
-
脳卒中後に生じる筋力低下の要因のうち、中枢神経系の問題以外に、筋組織そのものに生じる構造的変化を教えてください。
-
Grayらのレビューによると、主に以下の3つの構造的変化が挙げられます。
-
「長さ-張力関係」の静的モデルと動的モデルの違いは?
-
最も重要な違いは、最大の力を発揮できる「至適長」が固定的か、筋の活動レベルに応じて変動するかという点です。
-
カルシウム感受性の役割: Zimmermannらのレビューで示されているように、「長さ依存性の活性化」が生じる主な生理学的メカニズムは何ですか?なぜ筋が伸張されると、より低い活動レベルでも効率的に力を発揮できるようになるのか、ミオフィラメントレベルで説明してください。
-
主なメカニズムは、筋の伸張に伴うカルシウム感受性の増大です。ミオフィラメントレベルでは、筋が伸張されるとアクチンとミオシン間の距離が縮まります。これにより、少量のカルシウムイオンでも効率よく結合してクロスブリッジを形成できるようになるため、低い活動レベルでも力を発揮しやすくなります。
参考文献
3)Bohm S et al.:Assessment and modelling of the activation-dependent shift in optimal length of the human soleus muscle in vivo. 1371-1384, John Wiley & Sons Ltd on behalf of The Physiological Society, 2024.
KNERC 橋谷裕太郎(理学療法士)
